Au sein du Service d’Anatomie Pathologique de l’Institut Jules Bordet, les experts pathologistes se tournent de plus en plus vers la pathologie digitale, un outil « e-santé » véritablement indispensable pour analyser les tumeurs et le microenvironnement tumoral.
Il s’agit de la digitalisation des lames de microscopie sur lesquelles sont disposés des prélèvements (pièces opératoires, biopsie, prélèvements cytologiques, hématologiques, …). 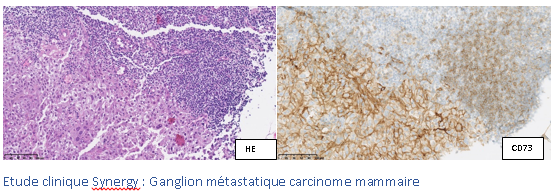
La numérisation de ces lames s’effectue grâce à des scanners dernière génération, à la pointe de la technologie. C’est le fruit d’un travail commun entre pathologistes et informaticiens qui permet la mise en place et la maitrise de ces « microscopes modernes ». Ceux-ci sont capables de numériser, d’annoter et de classer les lames sur des plateformes facilement accessibles et totalement sécurisées. La pathologie digitale facilite le travail minutieux d’analyse de cellules et de tissus biologiques qui fait le quotidien des pathologistes. Le service d’Anatomie Pathologique de l’Institut Jules Bordet est complètement intégré dans ce mouvement, une nouvelle étape dans la gestion et l’informatisation des données.
La pathologie digitale a plusieurs avantages :
- Elle permet un stockage d’images morphologiques dans le temps plus efficient et plus qualitatif. Les lames sont numérisées et ne doivent plus être conservées de manière physique, ce qui permet d’éviter la perte de qualité des lames (dû au temps qui passe).
- Elle représente l’avenir de l’histopathologie (l’analyse au microscope des tissus), un diagnostic plus précis grâce aux différentes possibilités qu’offre l’intelligence artificielle.
- Elle permet le partage aisé et sécurisé des données avec d’autres experts, pour un avis médical, même à l’autre bout du monde.
Les images digitales générées grâce au scanner du service d’Anatomie Pathologique de l’Institut Jules Bordet sont présentées, discutées et comparées aux images d’imagerie PET-FDG, CT, MR, … lors des Concertations Multidisciplinaires Oncologiques, où les experts se réunissent pour discuter des cas.
En cas de doute diagnostique, un deuxième avis peut être aussi sollicité à distance. C’est ce qu’on appelle la télépathologie, c’est-à-dire la possibilité de partager des informations à d’autres experts pour affiner le diagnostic. A l’Institut Jules Bordet, nos compétences sont également engagées pour la revue de différents cas d’études cliniques. Grâce au principe du cloud computing, le partage en ligne des lames virtuelles permet l’analyse des ressources provenant de laboratoires divers et/ou éloignés géographiquement. Les utilisateurs se connectent à un portail qui leur donne accès de manière contrôlée et sécurisée aux lames virtuelles. Ils peuvent les partager, les annoter, … directement en ligne.
Les pathologistes de l’Institut Jules Bordet ont pris l’habitude, avec le temps, de constituer des bibliothèques d’images digitales regroupant des cas intéressants.
La qualité d’image est optimale, le classement et l’accès sont rapides et faciles, évitant le désarchivage des lames en verre des archives (le service d’Anatomie Pathologique compte déjà des centaines de milliers des lames).
Ces cas rares servent aussi comme outil d’enseignement et de référence en cas de doute pour affiner un diagnostic.
Les lames digitales constituent un outil indispensable à la formation des jeunes pathologistes et pour les présentations dans le cadre de congrès et séminaires.
Par ailleurs, de nombreux outils sont intégrés aux lecteurs pour augmenter l’intérêt pédagogique ou diagnostique de la lame. Parmi ceux-ci, on peut évoquer la possibilité d’adjoindre des annotations ou des commentaires. Il est également possible de dépasser les limites du grossissement optique du microscope ou du scanner avec un zoom numérique. Un système « multi-fenêtres » permet de voir plusieurs lames simultanément : leur déplacement synchronisé est très utile pour observer plusieurs colorations différentes sur des champs.
Le scanner de lame est couramment utilisé dans nos activités et publications scientifiques, grâce à la bonne résolution de l’image et la possibilité d’annoter les composants tissulaires.
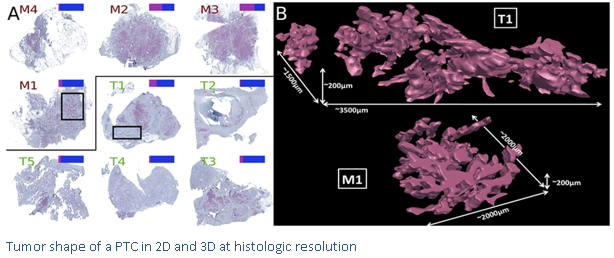
On peut également citer les projets de visualisation ultra-rapide des lames virtuelles en trois dimensions grâce à la numérisation de centaines de coupes tissulaires successives pour explorer l’image produite dans son épaisseur. Ce type d’analyse permet de rendre compte du volume des structures analysées par le pathologiste, et non simplement de leur surface.
Les pathologistes de l’Institut Jules Bordet, conjointement avec les chercheurs et bio-informaticiens, réalisent l’analyse de lames digitales sur de grands écrans en haute définition. Le pathologiste peut ainsi faire des annotations très fines, indispensables actuellement en transcriptomique spatiale. Cette technique permet d’analyser l’expression de gènes en quelques centaines de points au sein d’une coupe de tissu. Concrètement, il s’agit des microarrays de petite taille (6 × 6 mm2) comportant un millier de plots. Chaque plot donne une information sur l’ensemble des gènes exprimés, alors que l’hybridation in situ n’examine qu’un seul gène à la fois. La localisation de ces spots sur la lame par le pathologiste est essentielle à l’analyse de résultats.
Le scanner de lames est donc un outil qui, avec la participation des experts, pourrait automatiser des travaux, favorisant l’évolution vers l’Intelligence Artificielle. L’information mise au service du pathologiste est concentrée, fiabilisée et rend le diagnostic plus rapide et plus précis. Les nombreuses recherches en analyse d’images visent à étudier la validité de ces algorithmes sur une grande variété d’images. Notre service est activement impliqué dans deux réseaux, USA (FDA) et européen (TIGER).
Afin de parfaire nos analyses, nous sommes équipés d’un logiciel de traitement d’images digitales. Des nombreuses applications sont désormais disponibles : notamment la quantification des TILs par population, le scoring ki67, la détection de zones tumorales, mesure de superficies…. Ces applications peuvent être utilisées en recherche mais aussi pour compléter ou vérifier un diagnostic.
Recherche
Publications, présentations à des congrès, projets...
Virtual ESMO Annual 2020 congress
First findings from SYNERGY, a phase I/II trial testing the addition of the anti-CD73 oleclumab to the anti-PD-L1 durvalumab and chemotherapy as 1st line therapy for patients with metastatic triple-negative breast cancer
D. Eiger, C. Maurer, M. Brandão, P. Aftimos, K. Punie, D.Taylor, T. Van den Mooter, R.Poncin, JL. Canon, F. Duhoux, V. Casert, F. Clatot, C.Velghe, L. Craciun, M. Paesmans, E. de Azambuja, M. Ignatiadis, D. Larsimont, M. Piccart-Gebhart, L. Buisseret
Best oral presentation-Belgian Week of Pathology 2021
Implementation of automatic quantification of Ki-67 in well- differentiated gastro-entero-pancreatic neuroendocrine tumors: towards standardized evaluation into daily practice.
F. Lifrange, N. Gumus, L. Craciun, M. Gomez Galdon, P. Demetter, L. Verset.
Breast 2020 Dec; 54:179-186
Digital analysis of distant and cancer-associated mammary adipocytes.
E. Isnaldi, F. Richard, M. De Schepper, D. Vincent, S. Leduc, M. Maetens, T. Geukens, G. Floris, G. Rouas, F. Cardoso, C. Sotiriou, G. Zoppoli, D. Larsimont, E. Biganzoli, C. Desmedt.
J Clin Endocrinol Metab 2018
Distinctive Desmoplastic 3D Morphology Associated With BRAFV600E in Papillary Thyroid Cancers.
M. Tarabichi, A. Antoniou, S. Le Pennec, D. Gacquer, N. de Saint Aubain, L. Craciun, T. Cielen, I. Laios, D. Larsimont, G. Andry, JE. Dumont, C. Maenhaut, V. Detours.
San Antonio Breast Cancer Symposium 2021
Unravelling spatial tumor organization and heterogeneity in lobular breast cancer using spatial transcriptomics.
L. Collet, M. Serra, M. Rediti, F. Lifrange, D. Venet, X. Wang, D. Vincent, G. Rouas, D. Fimereli, D. Gacquer, AJ. Garcia, I. Veys, L. Craciun, D. Larsimont, M. Vikkula, F. Duhoux, F. Rothé, C. Sotiriou.
San Antonio Breast Cancer Symposium 2021
Integrating spatial transcriptomics and high-resolution morphological annotation to investigate tumor heterogeneity and PAM50 molecular subtyping in lobular breast cancer.
M. Serra, L. Collet, M. Rediti, F. Lifrange, D. Venet, X. Wang, D. Vincent, G. Rouas, D. Fimereli, D. Gacquer, AJ. Garcia, I. Veys, L. Craciun, D. Larsimont, M. Vikkula, F. Duhoux, F. Rothé, C. Sotiriou.
Molecular and Cellular Endocrinology 2022
Thyroid cancer under the scope of emerging technologies.
M. Tarabichi, P. Demetter, L. Craciun, C. Maenhaut, V. Detours.
NCI
Year 3: High-throughput truthing of microscope slides to validate artificial intelligence algorithms analyzing digital scans of pathology slides: data collection to create the medical device development tool (MDDT).
S.N Dudgeon, S. Wen, M. G Hanna, R. Gupta, M. Amgad, M. Sheth, H. Marble, R. Huang, M. D Herrmann, C. H Szu, D. Tong, B. Werness, E. Szu, D. Larsimont, A. Madabhushi, E. Hytopoulos, W. Chen, R. Singh, S. N Hart, A. Sharma, J. Saltz, R. Salgado, B. D Gallas.
J Pathol Inform 2021
A pathologist-annotated dataset for validating artificial intelligence: A project description and pilot study.
S. N Dudgeon, S. Wen, M. G Hanna, R. Gupta, M. Amgad, Ma. Sheth, H. Marble, R. Huang, M. D Herrmann, C. H Szu, D. Tong, B. Werness, E. Szu, D. Larsimont, A. Madabhushi, E. Hytopoulos, W. Chen, R. Singh, S. N Hart, A. Sharma, J. Saltz, R. Salgado, B. D Gallas.
BMC Cancer 2020
Retrospective analysis of the immunogenic effects of intra-arterial locoregional therapies in hepatocellular carcinoma: a rationale for combining selective internal radiation therapy (SIRT) and immunotherapy.
L. Craciun, R. de Wind, P. Demetter, V. Lucidi, A. Bohlok, S. Michiels, F. Bouazza, M. Vouche, I. Tancredi, G. Verset, S. Garaud, C. Naveaux, M. Gomez Galdon, K. Willard Gallo, A. Hendlisz, I. Duran Derijckere, P. Flamen, D. Larsimont, V. Donckier.